Kunci Jawaban IPA Kelas 10 Halaman 84: Partikel Subatom
Pada kesempatan kali ini, kita akan membahas kunci jawaban dari soal IPA Kelas 10 halaman 84 yang terdapat dalam Bab 3 berjudul "Struktur Atom". Materi yang dibahas adalah tentang partikel subatom yang menyusun atom. Kunci jawaban ini diharapkan dapat menjadi alternatif jawaban bagi siswa dalam menyelesaikan tugas mereka.
Soal pada halaman tersebut mengajak siswa untuk mengisi kolom yang kosong pada Tabel 3.2 yang berisi informasi tentang lambang atom dan ion. Setelah mengisi tabel tersebut, siswa diminta untuk menarik kesimpulan mengenai partikel subatom yang menyusun atom.
Berikut adalah kunci jawaban dan penjelasan lengkapnya:
Tabel 3.2 Lambang Atom dan Ion
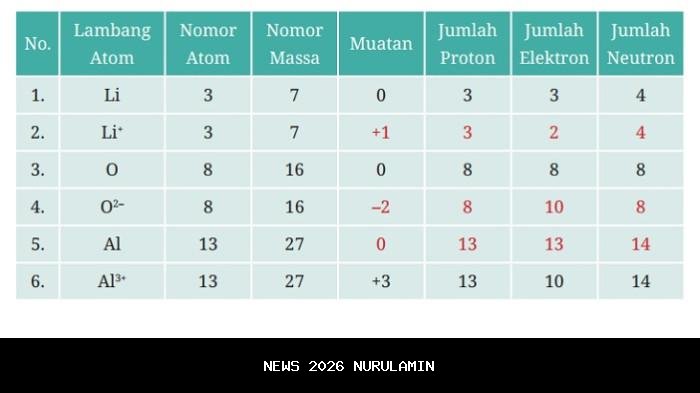
Dalam tabel tersebut, siswa diminta untuk mengisi informasi mengenai lambang atom, nomor atom (Z), nomor massa (A), jumlah proton, neutron, dan elektron. Setelah mengisi tabel, siswa dapat menarik kesimpulan bahwa partikel subatom yang menyusun atom adalah proton, neutron, dan elektron.
Pengertian Lambang Atom, Ion, dan Isotop
Lambang atom, ion, dan isotop merupakan cara untuk merepresentasikan atom berdasarkan partikel subatomiknya. Berikut penjelasannya:
-
Lambang Atom (Lambang Unsur)
Pengertian: Simbol standar untuk suatu unsur kimia, biasanya satu atau dua huruf dari nama Latinnya (huruf pertama kapital).
Contoh: O (Oksigen), C (Karbon), H (Hidrogen).
Notasi umumnya adalah $^A_ZX$, di mana X adalah lambang unsur, Z adalah nomor atom (proton), dan A adalah nomor massa (proton + neutron). -
Ion
Pengertian: Atom atau molekul yang kehilangan atau mendapatkan elektron sehingga memiliki muatan listrik bersih (positif atau negatif).
Jenis & Notasi: - Kation (Ion Positif): Atom kehilangan elektron.
-
Anion (Ion Negatif): Atom menerima elektron.
Perubahan: Hanya jumlah elektron yang berubah, bukan proton atau neutron. -
Isotop
Pengertian: Atom-atom dari unsur yang sama (nomor atom/proton sama), tetapi berbeda nomor massa (jumlah neutron berbeda).
Ciri: Memiliki sifat kimia mirip karena jumlah proton sama, tetapi massa berbeda.
Contoh: Karbon-12 dan Karbon-14 adalah isotop Karbon; keduanya punya 6 proton, tapi C-14 punya 8 neutron (14-6) dan C-12 punya 6 neutron (12-6).
Kesimpulan
Dari pembahasan di atas, dapat disimpulkan bahwa partikel subatom yang menyusun atom adalah proton, neutron, dan elektron. Proton dan neutron terletak di inti atom, sedangkan elektron bergerak di sekitar inti. Selain itu, atom dapat membentuk ion dengan kehilangan atau menerima elektron, serta memiliki variasi dalam bentuk isotop akibat perbedaan jumlah neutron.
Kunci jawaban ini diharapkan dapat membantu siswa memahami konsep dasar struktur atom dan partikel subatom. Namun, perlu diperhatikan bahwa kunci jawaban ini hanya sebagai alternatif, dan siswa tetap dianjurkan untuk memahami konsep secara mendalam.











Diskusi Pembaca
Belum ada komentar
Jadilah yang pertama memberikan tanggapan!
Tambah Komentar